本文將就靈芝多糖體研究的重要歷程進行分析報導,除了說明具備抗腫瘤、免疫增強、降血糖、免疫調節、抗氧化等作用的多糖體之間發現的經過與組成構形上的差異外,更期待能增進消費者在選擇靈芝產品的基本判斷能力。
文/許瑞祥
◎本文原載於2005年10月《健康靈芝》第30期28~33頁
現今的保健食品市場猶如戰國時代,經由媒體的強力放送,產品說明廣告不斷推陳出新,各種泛科學化的用語與模糊的功能訴求,常常會讓大眾在認知的過程中出現嚴重的困擾。
感覺上各種保健食品的作用都是相似的,彼此間是可以替代的,因此造就產品有流行的趨勢,每隔一段時間,新名詞、新包裝的產品出籠,消費者除了必須擴大支出應付之外,被迫追逐流行的代價如果破財又傷身將情何以堪?!
要選擇長期使用的保健食品,必須有嚴格的專業評估與長期的安全性調查,絕非新潮時髦可以替代。畢竟內服不比外用,連續長期大量使用的結果必定會增加其風險,因此作為健康食品的來源,其安全性應為首要考慮。
靈芝自古流傳為《本經》上品的高貴藥材,70 年代經大量人工栽培生產後,廣為民間研究開發利用。由於其傳承的藥效明確,已被列入 2000 年版《中華人民共和國藥典》中,靈芝與紫芝的子實體從此成為法定的中藥材。同時中國衛生部基於靈芝長期使用的經驗,批准靈芝作為食品的新資源,使靈芝成為藥食兼用的最佳代表。在《美國草藥藥典與治療概要》中亦將靈芝收錄於十種天然藥物之列,顯示靈芝受到美國醫藥學界的重視。
從古至今有關靈芝的敘述已經延續二千年,它不但沒有古文明的沒落與凋零,反而在現代科學化的檢驗中不斷展現其璀璨的內涵,讓西方國家學者驚豔,紛紛投入研究靈芝的行列中。從 NCBI 網頁中搜尋有關靈芝研究的期刊論文,近年來已有大量劇增的趨勢。靈芝產品能在國際市場中創造 25 億美元的市場價值,絕對是有其道理的。
在接觸靈芝的過程中,多糖體是最為人們熟悉的名詞之一,在廣告的強力放送下,多糖體似乎成為靈芝功效的代名詞,認識多糖體成了瞭解靈芝的基本常識。因此本文將就靈芝多糖體研究的重要歷程進行分析報導,除了說明具備抗腫瘤、免疫增強、降血糖、免疫調節、抗氧化等作用的多糖體之間,發現的經過與組成構形上的差異外,更期待能增進消費者在選擇靈芝產品的基本判斷能力。
70 年代人類健康最大的挑戰是癌症死亡率的不斷上升,擁有仙草光環的靈芝自然被用於抗癌的聖戰中,癌症患者使用靈芝來延長生命的事實,讓從事西方醫學訓練的藥理學家重新面對此一神奇的藥材並展開系列的探討。在此謹根據個人收藏的文獻,描述多糖體從發現到確認的過程。
1971 年日本學者 Sasaki 等人發表從野生樹舌靈芝(Ganoderma applanatum)子實體中萃取具有抗肉瘤(S-180)細胞於小鼠體內增生的活性成分,並認為具有β(1→3)鍵結主鏈的葡萄糖聚合物為其抗腫瘤活性的主要成分後,開始引起靈芝多糖體研究的風潮。
1977 年 Ito 等首先發表從人工栽培的靈芝(G. lucidum)子實體中分離所得的多糖體,經小鼠接種肉瘤(S-180)細胞株之模式確認其具有明顯的抗腫瘤活性,為栽培靈芝子實體的開發應用提供藥理研究的證據。
1981 年 Miyazaki 等人發表自靈芝子實體萃取後部分純化的抗腫瘤多糖體 GL-1 的基本組成,其分子量約 4 萬,主要由葡萄糖、木糖和阿拉伯糖以 18.8:1.5:1.0 的比例組成。可見其為以葡萄糖為主的雜多糖,具有 D-glucopyranosyl(1→4)α和(1→6)β 鍵結的主鏈和(1→3)β 鍵結葡萄糖支鏈。
此水溶性的多糖體 GL-1 經皮下注射(20mg/kg)10 天後對於小鼠體內的 S-180 肉瘤生長抑制率可達 95.6∼98.5%,顯示作者對於靈芝多糖體組成的複雜性已有深入的了解,分離純化具有不同活性多糖體的方法已經建立。
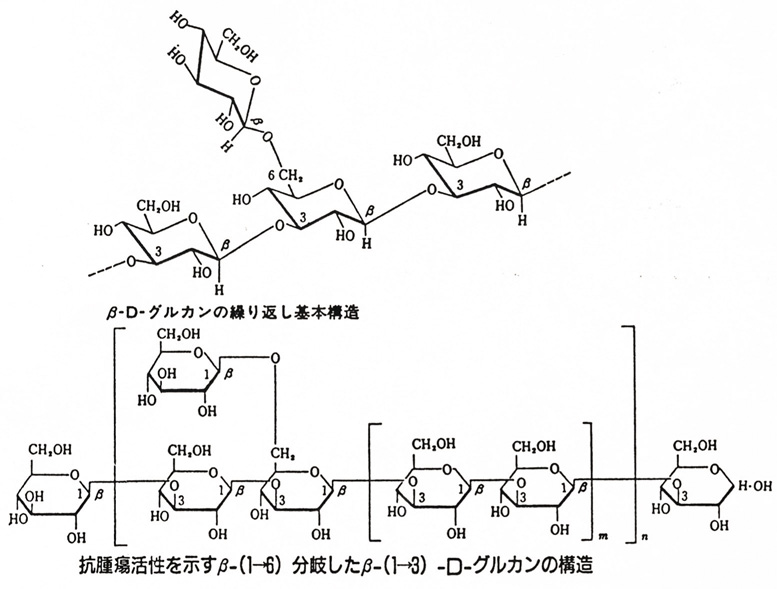
1981 年 Usui 等人發表從樹舌靈芝分離出二種抗腫瘤活性的多糖體,皆為熱水可溶的 β-D-glucan 是具有 β(1→3)鍵結主鏈與 β(1→6)鍵結分支的葡聚糖。其中分子量1,050,000的 G-l-2a-β 具有最強的抗腫瘤活性,在小鼠接種 S-180 的評估模式中 ID50 值為 0.15 mg/kg,每天注射 1mg/kg 時,可達100%的腫瘤抑制率。此 β-D-glucan 即為大家最熟悉的高分子多糖體活性構形的基本組成。
1980 年韓國漢城大學金炳鈺教授主持的研究室,亦開始發表系列有關韓國產靈芝抗癌成分之研究報告,相較於日本學界提取多糖常用的熱水萃取法,韓國文獻中較多以稀鹼溶液來萃取多糖體。
將 100 公克的靈芝子實體經 0.1N NaOH 溶液萃取後,可得約 9.9 公克的多糖體。其組成分析為含有 72.5% glucose、15.8% manose、8.3% galactose、3.4% xylose 和 18 種胺基酸的蛋白多糖體。每日皮下注射 50mg/kg 對接種 S-180 肉瘤的小鼠在 28 天的試驗中,其腫瘤抑制率為 87.6%,其中約有三分之一小鼠腫瘤完全消失。
日後依循此萃取模式的多糖體,在韓國靈芝研究的領域中,具有關鍵性的影響。
1982 年台北醫學院鄭惠華教授等發表,從太空包培養的靈芝子實體經熱水萃取後所得的粗抽出物,在小鼠接種 S-180 細胞前一週與接種後一天,每天經皮下注射相同劑量的靈芝抽出物,在 20 天的試驗結果顯示,提前一週使用者約有 80∼100% 的腫瘤抑制效果,於接種一天後才開始注射者腫瘤消失比例約為 40∼60%。但若是以相同劑量經胃管餵食者,則無抑制肉瘤的作用。
此篇為國內首見靈芝抗癌研究的先鋒,雖未提及多糖體的分離,但卻闡釋靈芝用於預防勝於治療的意義。
同年郭明德等發表以無柄靈芝(G. resinaceum)菌絲體及培養液,經熱水萃取及四倍體積酒清沈澱的部分,對接種 S-180 肉瘤細胞的 ICR 小鼠體內腫瘤的生長,有明顯的抑制作用,同時並可延長其存活的時間。本篇論文開啟國內研究菌絲體抗腫瘤的風氣。
1984 年陽明大學李旭生教授等開始發表,人工培養靈芝(G. lucidum)菌絲體熱水萃取物抗腫瘤研究的系列成果。經由腹腔注射萃取物對於 C3H 鼷鼠皮下移植之纖維肉瘤細胞的生長具有抑制作用,在以尾靜脈注射纖維肉瘤細胞引起肺部轉移病灶的評估模式中,亦顯示此靈芝菌絲體萃取物對於抑制惡性腫瘤的轉移具有明顯效果。
本文不但證實靈芝菌絲體具有抗腫瘤活性,同時也提供靈芝能抑制癌細胞遷移的具體證據。
1984 年,日本靜岡大學水野卓教授亦開始發表系列靈芝多糖體的論文。首先發表從靈芝(G. lucidum)子實體經熱水萃取、酒精沈澱、管柱層析後部分純化的活性多糖體,分子量分別為 1,050,000 和 450,000。
其中分子量 1,050,000的β-D-glucan,是以 β(1→3)鍵結為主鏈、含有分歧頻度 4 的β(1→6)鍵結、由 6 個糖連結的短支鍵構造,此多糖體經接種 S-180 細胞的 ICR/Jcl 小鼠模式在 25 天的試驗中所得的半數抑制量(ID50)為 8 mg/kg;分子量為 450,000 的酸性多糖其 ID50 為 22 mg/kg。
就此同一時期所發表文獻內容而言,日本學者在多糖的分離純化與組成分析技術較為完整,對其所用於抗腫瘤試驗的多糖體大小與鍵結方式有較精確的記載,提供日後對於活性多糖體定義時的重要參考。
1985 年 Sone 等人發表同時自靈芝子實體和菌絲體中,經熱水或稀鹼溶液萃取而得各種多糖體之間抗腫瘤活性的比較。大部分的水不溶性多糖體具有 β(1→3)鍵結的D-葡萄糖主鏈、β(1→6)鍵結支鏈和少數 β(1→4)鍵結的支鏈。
在各種多糖體的組成中,支鏈的分歧頻度由 1/3∼1/23 不等。熱水萃取子實體而得的多糖體(HW-2)與菌絲體的胞外多糖,對接種 S-180 小鼠具有較高的腫瘤抑制率,在 10 mg/kg 劑量下抑制率可達 96% 和 91%。
作者在文中強調,抗腫瘤活性與其多糖體側鏈分支的頻度有關,降低分支側鏈的多糖體,其抗腫瘤活性相對降低。本篇為同時比較子實體和菌絲體來源多糖體組成構形差異與抗腫瘤作用關係的代表作。
1989 年董大成教授的研究團隊發表系列有關口服靈芝菌絲體培養液的抗腫瘤效果,為日後靈芝產品口服的功效提供有利的佐證。
由黃雪芳等發表,以靈芝培養液餵食經尾靜脈注射 S-180 肉瘤細胞小鼠作為人工轉移癌細胞於肺臟的研究模式中發現,靈芝菌絲體培養液中的多糖體無論是經口服或皮下注射,皆能抑制癌細胞的肺臟轉移作用。
而劉柯俊等的研究結果則顯示,經同位素標幟的靈芝菌絲體培養液餵食 ICR 小鼠後,其血清和器官中皆可測得放射性活性升高的現象,尤其以肝臟最為顯著。將此培養液與小鼠腹腔巨噬細胞共同培養一小時後,發現巨噬細胞攝入具放射性活性的物質。
作者推論,口服靈芝的多糖體可能經由腸道上皮絨毛細胞之胞飲或腸管內的吞噬細胞所攝入後,產生與注射入體內相似的抗腫瘤效果。
1993 年 Wang 等發表以松杉靈芝(G. tsugae)子實體來源的多糖體,經系列的分離與純化後進行抗腫瘤活性評估,在其所得的 14 種水溶性多糖與 15 種水不溶性多糖中,發現只有7種具有抗腫瘤(S-180)活性,皆是由 β(1→3)-D-glucan 為主鏈,並且含有部分蛋白質的糖蛋白聚合物,同時作者亦比較三種具有抗腫瘤活性的靈芝、樹舌靈芝、松杉靈芝間的多糖體組成與抗 S-180 肉瘤活性的評估。
以松杉靈芝為抗腫瘤研究材料的文獻正式誕生,在一向以 G. lucidum 為學名發表靈芝藥理研究成果中,本文使用松杉靈芝為研究對象,更是要彰顯不同物種間多糖組成的歧異,同時亦可瞭解在眾多的多糖構形間,抗腫瘤活性也有極大的落差,對於有效的活性多糖能有更明確的界定。
1994 年 Zhang 等接著發表松杉靈芝菌絲體 25 公斤以熱水萃取後所得的 450 公克水可溶多糖體,經離子交換與親和性管柱層析後,可得 16 種多糖,其中 3 種為具有抗 S-180 細胞於小鼠體內增生的活性多糖體,分子量在 10,000∼16,000 之間,並具有 5.8%∼9.3% 的蛋白質。
在以相同劑量(10 mg/kg)注射於接種 S-180 細胞的小鼠評估試驗結果顯示,與子實體來源分子量相同的多糖體(F1o-a)比較,其腫瘤抑制率較低。
本文比較由松杉靈芝子實體和菌絲體萃取所得分子量相同的多糖體,具有明顯不同的抗腫瘤活性,顯示相同物種在不同的生理階段所累積的代謝產物,功能差異很大。因此在不同原料的基礎上,所謂多糖體的含量、組成與效果間,是無法互相推論或引用的。
1995 年北京醫科大學林志彬教授發表靈芝子實體中提取的多糖肽,不僅能抑制小鼠接種肉瘤(S-180)生長,並可抑制小鼠體內 Lewis 肺癌細胞生長,在每天注射 50mg/kg 劑量下,其抑制率可達 55%。
另外,以靈芝多糖 B(50、100、200 mg/kg/day)灌胃 10 天觀察結果均可抑制 S-180 細胞的生長,其抑制率分別為 28%、56%、67%;若合併抗腫瘤藥 cyclophosphamide 的使用,能明顯增強其抗腫瘤作用。
從 1970~1995 年的文獻資料中顯示,靈芝對於試驗動物的移植性腫瘤具有生長抑制作用,並可使瘤的重量減輕,延長寄主動物生存的時間,而多糖體,尤其是具有 β(1→3)主鏈的 D-glucan,是其抗腫瘤的重要有效成分。
在活體內使用具有抗腫瘤活性的多糖體,是直接殺死癌細胞,還是經由激發寄主體內抗腫瘤機制間接殺死癌細胞,抗腫瘤作用的機制成為學術討論的焦點,從此並將靈芝研究的模式從動物推展至細胞株,從腫瘤細胞到免疫細胞,由體內到體外實驗。
有關直接殺死腫瘤細胞的體外試驗,無論是以高劑量的靈芝萃取物直接添加於 S-180 的細胞培養液中,對其細胞增殖無抑制作用,或是以靈芝多糖 B 200 μg/ml、菌絲體多糖 750 μg/ml 直接加入人類白血病細胞株(HL-60)培養液中,對 HL-60 細胞的生長亦無直接的抑制作用,同時也不能誘導細胞的凋亡。
到底靈芝多糖體是如何發揮抗腫瘤作用的,在 1997 年榮總王聲遠教授發表靈芝與免疫調節的研究成果後,靈芝多糖體的抗腫瘤機制才逐漸被確認,同時開啟靈芝與免疫系統精彩研究的序幕。
王教授等發表以高劑量靈芝子實體多糖(PS-G)400 μg/ml 添加於白血病細胞株 HL-60 和 U937 的培養液中,並不會造成細胞的死亡或凋亡。將 PS-G 100 μg/ml 添加於巨噬細胞的培養液中時,其中的介白素 1β(interleukin 1β)、TNF-α(tumor necrosis factor-α)和 IL-6 的含量較未添加處理的控制組增高 5.1、9.8 和 29 倍。而以 PS-G 添加的 T 淋巴細胞(T-lymphocytes)培養液中,IFN-γ 的含量亦大幅度提升。
在此將培養上清液施用於 HL-60 與 U937 的細胞培養液中時,明顯可誘導白血病細胞株的凋亡(apoptosis),此外有 40~45% 的白血病細胞分化成為具有 CD14 和 CD68 表面抗原的成熟單核球細胞。
本篇首次從細胞激素(cytokines)的證據說明,靈芝多糖能抑制腫瘤細胞的增殖作用,是透過免疫系統中的巨噬細胞和T淋巴細胞產生的 TNF-α 和 IFN-γ 協同作用的結果。(待續)
COPYRIGHTS © Ganodermanews SINCE By 2015 ALL RIGHT RESERVED.
靈芝新聞網 版權所有 | 本網站內容作者享有其著作權,禁止侵害,違者必究
Powered by
ganodermanews.com